Изготовление инъекционных растворов в аптеке (стр. 2 из 3)
Приготовление инъекционных растворов без стабилизаторов
2.1 Приготовление инъекционных растворов без стабилизаторов
Приготовление инъекционных растворов без стабилизаторов складывается из следующих последовательных операций:
— расчет количества воды и сухих лекарственных веществ;
— отмеривание необходимого количества воды для инъекций и отвешивание лекарственных веществ;
— подготовка флакона и укупорочных средств;
— оценка качества инъекционного раствора;
— оформление к отпуску;
Rp.: Solutionis 25% 30ml
Da. Signa: по 1мл внутримышечно 3 раза в день
Выписан раствор вещества, хорошо растворимого в воде, для парентерального применения.
Воды для инъекций
30 – (7,5х0.68) = 34,56мл
0,68 – коэффициент увеличения объема анальгина
Создание асептических условий достигается приготовлением инъекционных лекарственных средств из стерильных медикаментов, в стерильной посуде и в специально оборудованном помещении. Однако асептика не может гарантировать полную стерильность растворов, поэтому они в дальнейшем подвергаются стерилизации.
При расчете количества воды для инъекций необходимо учитывать, что концентрация анальгина превышает 3% и поэтому необходимо учитывать коэффициент увеличения объема.
В асептическом блоке в стерильной подставке в 34,65мл свежеперегнанной воды для инъекций растворяют 7,5г анальгина. Приготовленный раствор фильтруют через двойной стерильный бензольный фильтр с комочком длинноволокнистой ваты. Можно для фильтрации использовать стеклянный фильтр №4. раствор фильтруют в стерильный флакон объемом 50мл из нейтрального стекла.
Укупоривают флакон стерильной резиновой пробкой и обкатывают металлическим колпачком. Проверяют раствор на прозрачность, отсутствие механических включений, цветность. Затем раствор стерилизуют в автоклаве при 120°С 8 минут. После стерилизации и охлаждения раствор передают на контроль повторно.
Флакон прозрачного стекла укупорен герметично резиновой пробкой «под обкатку», наклеивают номер рецепта и этикетки: «Для инъекций», «Стерильно», «Хранить в прохладном и защищенном от света месте», «Беречь от детей».
2.2 Приготовление инъекционных растворов со стабилизатором
При изготовлении инъекционных растворов необходимо принимать меры к обеспечению сохранности лекарственных веществ.
Стабильность — это неизменность свойств содержащихся в растворах лекарственных веществ — достигается подбором оптимальных условий стерилизации, использованием консервантов, применением стабилизаторов, соответствующих природе лекарственных веществ. Несмотря на многообразие и сложность процессов разложения лекарственных веществ, наиболее часто имеют место гидролиз и окисление.
Лекарственные вещества, требующие стабилизации их водных растворов, можно разделить на три группы:
1) соли образованные сильными кислотами и слабыми основаниями;
2) соли, образованные сильными основаниями и слабыми кислотами;
3) легкоокисляющиеся вещества.
Стабилизация растворов солей сильных кислот и слабых оснований (соли алкалоидов и азотистых оснований) осуществляется добавлением кислоты. Водные растворы таких солей вследствие гидролиза имеют слабокислую реакцию. При тепловой стерилизации и хранении таких растворов рН повышается ввиду усиления гидролиза, сопровождающегося уменьшением концентрации водородных ионов. Сдвиг рН раствора приводит к гидролизу солей алкалоидов с образованием мало растворимых оснований, которые могут выпадать в осадок.
Прибавление к растворам солей сильных кислот и слабых оснований свободной кислоты подавляет гидролиз и таким образом обеспечивает стабильность инъекционного раствора. Количество кислоты, необходимое для стабилизации растворов солей, зависит от свойств вещества, а также оптимальной границы рН раствора (обычно рН 3,0—4,0). 0,1 н раствор хлористоводородной кислоты используют для стабилизации растворов дибазола, новокаина, спазмолитика, совкаина, атропина сульфата и др [4].
Rp.: Solutionis Dibazoli 1% 50ml
Da. Signa: по 2 мл 1 раз в день подкожно
Выписана жидкая лекарственная форма для инъекционного применения, представляющая собой истинный раствор, в состав которого входит вещество группы Б.
хлористоводородной 0,1 и
Воды для инъекций до 50 мл
В рецепте пописан раствор для подкожного введения, в состав которого входит вещество, трудно растворимое в воде. Инъекционные растворы дибазола нуждаются в стабилизации 0,1н хлористоводородной кислоты.
В асептических условиях в стерильной мерной колбе емкостью 50мл в части воды для инъекций растворяют 0,5г дибазол, добавляют 0,5 0,1н раствора хлористоводородной кислоты м доводят водой до метки. приготовленный раствор фильтруют в склянку для отпуска емкостью 50мл из нейтрального стекла через двойной стерильный беззольный фильтр с подложенным комочком длинноволокнистой ваты.
Флакон укупоривают и проверяют раствор на отсутствие механических примесей, для чего склянку переворачивают вверх дном и просматривают в проходящем свете на черно-белом фоне. Если при просмотре обнаруживаются механические частицы, операцию фильтрации повторяют. Затем горловину склянки с пробкой обвязывают стерильной и еще влажной пергаментной бумагой с удлиненным концом 3х6см, на котором ассистент должен сделать запись графитным карандашом о входящих ингредиентах и их количестве, и поставить личную подпись.
Склянку мс приготовленным раствором помещают в бикс и стерилизуют при 120°С 8 минут. После охлаждения раствор передают на контроль.
Aquae pro injectionibus
Hidrychloridi 0,1 № 50ml
Стабилизация солей сильных оснований и слабых кислот осуществлется добавлением щелочи или натрия гидрокарбоната. Растворы солей, образованных сильными основаниями и кислотами, диссоциируют с образованием слабодиссоциирующей кислоты, что влечет к уменьшению свободных ионов водорода, а, как следствие, к увеличению рН раствора. Для подавления гидролиза подобных растворов солей необходимо добавить щелочь. К числу солей, стабилизируемых едким натрием или натрия гидрокарбонатом, относятся: никотиновая кислота, кофеин-бензоат натрия, натрия тиосульфат, натрия нитрит.
Стабилизация растворов легковоспламеняющихся веществ. К легкоокисляющимся лекарственным веществам следует отнести аскорбиновую кислоту, натрия салицилат, сульфацил натрия, стрептоцид растворимый, аминазин и др.
Для стабилизации этой группы препаратов используют антиоксиданты — вещества, обладающие большим окислительно-восстановительным потенциалом, чем стабилизируемые лекарственные вещества. К этой группе стабилизаторов относятся: сульфит и метабисульфит натрия, ронгалит, аскорбиновая кислота и др. Другая группа антиоксидантов способна связывать ионы тяжелых металлов, катализирующих окислительные процессы. К ним относятся этилендиаминтетрауксусная кислота, трилон Б и др.
Растворы ряда веществ не могут приобрести необходимую устойчивость при использовании какой-либо одной формы защиты. В этом случае прибегают к комбинированным формам защиты. Комбинированную защиту используют для растворов сульфацила натрия, адреналина гидрохлорида, глюкозы, аскорбиновой кислоты и некоторых других веществ.
Тема: «Промышленное производство инъекционных растворов»

ТЕМА: «ПРОМЫШЛЕННОЕ ПРОИЗВОДСТВО ИНЪЕКЦИОННЫХ РАСТВОРОВ«
При выполнении заданий по данной теме прежде всего следует изучить фармакопейную статью ГФ XI вып 2, стр. 140 «Инъекционные лекарственные формы», в соответствии с которой необходимо знать требования предъявляемые к растворам, растворителям и исходным субстанциям. Особое внимание обратить на конструктивные особенности дистилляторов, позволяющих получать апирогенную воду, знать достоинства и недостатки методов получения. Необходимо так же знать методы микробиологического контроля растворов на стерильность, методики испытаний на пирогенность и токсичность, и фармакопейные методы стерилизации (см. ГФ XI стр. 19,182-183, 187).
Вопросы для самоподготовки
1Требование к флаконам и ампулам для инъекционных растворов
2.Ампульное стекло, его состав, показатели качества
3. Мойка и сушка стеклодрота
4. Выделка и отжиг ампул
5. Требования правил GMP к производству инъекционных растворов (к спец одежде персоналу, оборудованию, воздуху)
6. Мойка ампул (вакуумная, шприцевая, пароконденсационная)
7. Сушка и стерилизация ампул
8. Приготовление инъекционных растворов, стабилизация, дополнительная очистка
9.Фильтрование растворов. Фильтрующие материалы, требования, классификация, глубинное и мембранное фильтрование.
10.Вода апирогенная, требования, способы получения.
11. Наполнение ампул растворами.
12.Запайка ампул, контрль качества запайки.
13.Стериллизация инъекционных растворов: способы и режим стерилизации, контроль стерильности.
14.Оценка качества инъекционных растворов, способы определения механических включений.
15. Этикетировка, упаковка ампул
Перечень технологического оборудования.
1. Установка для мойки и сушки стеклодрота (камерные способы).
2. Аппараты для получения апирогенной воды: горизонтальный трехступенчатый, термокомпрессионый
3. Полуавтомат для выделки ампул.
4. Печь туннельного типа для отжига ампул.
5. Вакуум-моечный аппарат
6. Установка для пароконденсационной мойки ампул
7. Аппарат для шприцевой мойки ампул
8. Паровой стерилизатор АП-7
9. Фильтр ХНИХФИ и установка для фильтрования
10.Установка для наполнения ампул шприцевым способом
11.Автомат для запайки ампул
13.Принципиальная схема ампулирования инъекционных растворов в среде углекислого (инертного) газа
ОФС «ИНЪЕКЦИОННЫЕ ЛЕКАРСТВЕННЫЕ ФОРМЫ» (ГФ XI, вып.2, стр 140)
Лекарственные средства для парентерального применения
К лекарственным средствам для парентерального применения относятся стерильные водные и неводные растворы, суспензии, эмульсии и сухие твердые вещества (порошки, пористые массы, таблетки), которые растворяют в стерильном растворителе непосредственно перед введением. Растворы для парентерального применения объемом 100 мл и более относятся к инфузионным.
Лекарственные средства для парентерального применения готовят в условиях, максимально предотвращающих загрязнение готового продукта микроорганизмами и посторонними веществами.
Для приготовления лекарственных средств для парентерального применения используют лекарственные, вспомогательные вещества и растворители, разрешенные к медицинскому применению.
Лекарственные средства для парентерального применения должны быть стерильными, практически свободными от видимых механических включений, выдерживать испытания на пирогенность и токсичность в соответствии с требованиями частных статей. Инъекционные растворы могут быть изотоничными, изогидричными и изоионичными в соответствии с требованиями частных статей.
Растворители. В качестве растворителей применяют воду для инъекций, жирные масла, этилолеат. В составе комплексного растворителя могут быть использованы спирт этиловый, глицерин, пропиленгликоль, полиэтиленоксид 400, бензилбензоат, бензиловый спирт и другие растворители.
Вспомогательные вещества. При изготовлении лекарственных средств для парентерального применения могут быть добавлены консерванты, антиоксиданты, стабилизаторы, эмульгаторы, солюбилизаторы и другие вспомогательные вещества, указанные в частных статьях.
В качестве вспомогательных веществ используют аскорбиновую, соляную, винную, лимонную, уксусную кислоты, натрия карбонат, натрия бикарбонат, натр едкий, натрия или калия сульфит, бисульфит или метабисульфит, натрия тиосульфат, натрия цитрат, натрия фосфат одно — и двузамещенный, натрия хлорид, метиловый эфир оксибензойной кислоты, пропиловый эфир оксибензойной кислоты, ронгалит, динатриевую соль эти-лендиаминтетрауксусной кислоты, спирт поливиниловый, хлоро-бутанол, крезол, фенол и др.
Количество добавляемых вспомогательных веществ, если нет других указаний в частных статьях, не должно превышать следующих концентраций: для веществ, подобных хлорбутанолу, крезолу, фенолу,
— до 0,5%; сернистого ангидрида или эквивалентных количеств сульфита, бисульфита или метабисульфита калия или натрия — до 0,2 %.
Консерванты применяют в многодозовых лекарственных средствах для парентерального применения, а также в однодозовых препаратах в соответствии с требованиями частных статей.
Лекарственные средства для внутриполостных, внутрисердеч-ных, внутриглазных или других инъекций, имеющих доступ к спинномозговой жидкости, а также при разовой дозе, превышающей 15 мл, не должны содержать консервантов.
Сосуды и укупорочные средства должны обеспечивать герметичность, быть индифферентными к содержимому, сохранять его стабильность при стерилизации, хранении и транспортировании. Марки стекла и других укупорочных средств (резины, пластмассы) должны быть указаны в частных статьях. Сосуды изготавливают из материалов, не затрудняющих визуальный контроль содержимого.
Материал пробки должен быть достаточно прочным и эластичным, чтобы обеспечивать отбор содержимого без удаления пробки и отделения ее частиц и герметизацию сосуда после удаления иглы.
Прозрачность. Растворы должны быть прозрачными, по сравнению с водой для инъекций или соответствующим растворителем, если нет других указаний в частных статьях.
Окраска. Окраску лекарственных средств для парентерального применения определяют путем сравнения с эталонами цветности в соответствии со статьей «Определение окраски жидкостей» или указаниями частных статей.
Объем инъекционных растворов в сосудах должен быть больше номинального.
В сосудах вместимостью до 50 мл наполнение проверяют калиброванным шприцем, в сосудах вместимостью 50 мл и более — калиброванным цилиндром при температуре (20±2) °С.
Объем инъекционных растворов в сосудах
ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ РАСТВОРОВ ДЛЯ ИНЪЕКЦИЙ
Процесс изготовления состоит из следующих стадий:
1. Подготовительная, в том числе: проведение расчетов, подготовка условий асептического изготовления, мойка и стерилизация тары и упаковки, получение воды для инъекций.
2. Получение растворов для инъекций, в том числе операции: растворение, фильтрация, розлив, укупорка, проверка на отсутст-
вие механических включений, полный химический анализ, стерилизация.
3. Маркировка готовой продукции.
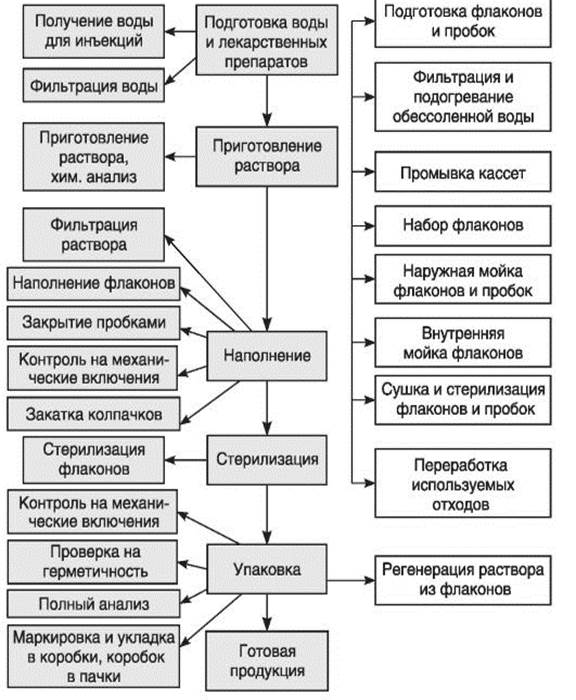
Типовая технологическая схема изготовления инъекционных растворов представлена на схеме 5.1. Технологический процесс изготовления разделяется на 3 потока:
— подготовка тары и упаковки;
— стерилизация, контроль качества, упаковка и маркировка готовой продукции.
Для получения растворов для инъекций и инфузий используют флаконы из нейтрального стекла марки НС-1 (для медицинских препаратов, антибиотиков) и НС-2 (сосуды для крови). В порядке исключения (после освобождения от щелочности) используют флаконы из стекла марки АБ-1 и МТО. Срок хранения растворов в них не должен превышать 2 сут.
При обработке флаконы из щелочного стекла заполняют водой очищенной, стерилизуют при температуре 120 ?С 30 мин. После обработки проводят контроль ее эффективности (потенциометрическим или ацидиметрическим методом). Изменение значения рН воды до и после стерилизации во флаконе не должно быть более 1,7.
Новую посуду снаружи и внутри обмывают водопроводной водой, замачивают на 20-25 мин в моющих растворах, подогретых до температуры 50-60 ?С. Используют также взвесь горчицы 1:20, 0,25% раствор «Дезмола», 0,5% растворы «Прогресса», «Лотоса», «Астры», 1% раствор СПМС (смесь сульфанола с натрия триполифосфатом 1:10). При сильном загрязнении посуду на 2-3 ч замачивают в 5% взвеси горчицы или растворе моющих средств в соответствии со специальной инструкцией.
Вымытую посуду стерилизуют горячим воздухом при температуре 180 ?С 60 мин. Посуду, бывшую в употреблении, дезинфицируют: 1% раствором активированного хлорамина — 30 мин; 3% свежеприготовленным раствором водорода пероксида с добавлением 0,5% моющих средств — 80 мин или 0,5% раствором «Дезмола» — 80 мин.
Для укупорки флаконов с инъекционными растворами используют пробки специальных сортов резины: ИР-21 (силиконовая); 25 П (натуральный каучук); 52-369, 52-369/1, 52-369/П (бутиловый каучук); ИР-119, ИР-119А (бутиловый каучук). Новые резиновые пробки
Схема 5.1.Типовая технологическая схема изготовления растворов
обрабатывают с целью удаления с их поверхности серы, цинка и других веществ в соответствии с инструкцией.
Пробки, бывшие в употреблении, промывают водой очищенной и кипятят в ней 2 раза по 20 мин, стерилизуют при температуре 121+2 ?С 45 мин.
Для изготовления растворов используют воду для инъекций (см. главу 21) и лекарственные средства квалификации «Для инъек- ций» или другие, если имеется указание в соответствующих ФС.
Фильтрование растворов для инъекций проводят через глубинные, чаще мембранные фильтры (см. главу «Асептика, стерилизация фильтрованием»).
В случае приготовления малых объемов инъекционных растворов применяют фильтр «Грибок» (рис. 25.13), представляющий собой воронку, обтянутую фильтровальным материалом, и работающий под разрежением. Фильтровальный пакет состоит из шелковой ткани в 2 слоя, фильтровальной бумаги в 3 слоя, марлевой прокладки и шелковой ткани в 2 слоя. Полностью заполненную воронку обвязывают сверху парашютным шелком. Фильтруют под вакуумом.
Профильтрованный раствор с помощью дозаторов разливают в подготовленные бутылки для инъекционных растворов. Закрывают пробками.
Флаконы с растворами для инъекций, укупоренные резиновыми пробками, контролируют на отсутствие механических включений. При обнаружении механических включений при первичном контроле раствора его перефильтровывают.
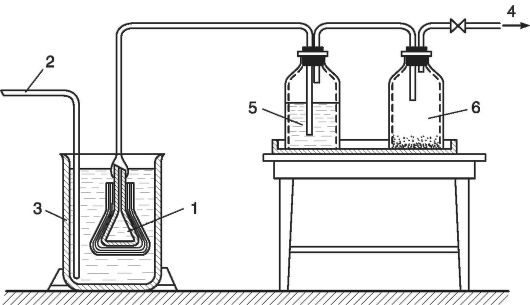
Рис. 5.13.Фильтр «Грибок»:
1 — воронка, обтянутся слоем фильтровальных материалов; 2 — линия подачи растворов; 3 — стакан с фильтруемым раствором; 4 — вакуум; 5 — приемник с профильтрованным раствором; 6 — ловушка на вакуумной линии
После изготовления растворы для инъекций подвергают химическому анализу, заключающемуся в определении подлинности (качественный анализ) и количественного содержания лекарственных веществ, входящих в состав лекарственной формы (количественный анализ). Количественному и качественному анализам провизоры-аналитики подвергают первично все серии инъекционных растворов, которые готовят в аптеке (до стерилизации). В аптеках, где нет провизора-аналитика, количественному анализу подвергают растворы атропина сульфата, новокаина, глюкозы, кальция хлорида и изотонический раствор натрия хлорида. Контроль путем опроса провизора-технолога проводят немедленно после изготовления инъекционного раствора. При положительном результате обкатывают металлическими колпачками.
Закатанные бутылки с растворами для инъекций маркируют по алюминиевому колпачку, указывая наименование, номер серии.
Маркированные флаконы помещают в автоклав и стерилизуют в соответствии с указаниями ГФ, учитывая объем раствора в сосуде. После стерилизации растворы анализируют на содержание механических включений в соответствии с приказом ? 308. Забракованные флаконы переработке не подлежат.
Отбракованные флаконы направляют на полный анализ в соответствии с требованиями ГФ или ФС.
Отбирают пробу на анализ стерильности и отсутствие пирогенных веществ. В случае положительного результата маркируют и упаковывают в гофрокоробки.
Изготовление растворов для инъекций
Регламентируется рядом НД:
— Приказами МЗ РФ № 309, 214, 308.
— МУ по изготовлению стерильных растворов в аптеках, утвержденных МЗ РФ от 24.08.94г.
Лекарственные формы для инъекций могут изготавливаться только в тех аптеках, которые имеют асептических блок и возможности для создания асептики. Не разрешается готовить инъекционные лекарственные формы, если нет методики количественного анализа, данных о совместимости ингредиентов, режиме стерилизации и технологии.
3.1. Стадии технологического процесса:
2. Изготовление раствора
7. Оформление к отпуску
3.2. Приготовление инъекционных растворов.
Инъекционные растворы изготавливают массо-объемным способом. В м е р н о й к о л б е в части воды растворяют лекарственные вещества, при необходимости добавляют вспомогательные вещества (стабилизаторы, изотонирующие вещества), раствор перемешивают и доводят растворителем до требуемого объема. При отсутствии мерной колбы больших объемов
для определения количества растворителя следует использовать КУО. Категорически запрещается одновременное изготовление на одном рабочем месте нескольких стерильных растворов, содержащих лекарственные вещества с различными наименованиями или одного наименования, но в разных концентрациях. После изготовления раствора заполняют ППК, берут пробу для полного химического контроля. Результаты анализа регистрируют в «Журнале регистрации результатов контроля отдельных стадий изготовления растворов для инъекций и инфузий» (приложение N5 пр.214). Количество взятых лекарственных и вспомогательных веществ записывается в журнале регистрации графа N4 и N5. После удовлетворительного результата анализа раствор фильтруют.
3.3. Фильтрование и фасовка растворов.
Одной из самых ответственных и трудоемких технологических операций является фильтрование растворов для инъекций.
В аптеках наиболее распространено фильтрование с помощью вакуума. В качестве фильтрующих материалов применяют комбинированные фильтры с применением медицинской ваты, лабораторной фильтровальной бумаги, хлопчатобумажной бытовой марли – после соответствующей обработки.
Для фасовки инъекционных растворов используют стерильные флаконы из нейтрального стекла марки НС-1, НС-2. Для укупорки применяют пробки из специальных сортов резины: силиконовые ИР-21, из нейтрального каучука 25П, бутилового каучука ИР-119.
Затем флакон укупоривают, проверяют на чистоту на белом и черном фоне в проходящем свете при помощи УК-2.
Чистый раствор подготавливают к стерилизации — обкатывают алюминиевым колпачком или обвязывают пергаментом, проводят проверку качества укупорки флаконов (алюминиевый колпачок не должен прокручиваться при проверке вручную, раствор не должен выливаться при опрокидывании), маркируют путем надписи или штамповке. На колпачке или ярлычке (3×6 из пергамента) пишется наименование раствора, концентрация. Передают на стерилизацию. Повторная стерилизация растворов для инъекций не допускается. После стерилизации раствор подвергаются контролю на чистоту, герметичность и проводится полный химический анализ действующих веществ.
3.4. Стандартизация.
Стерильные растворы считаются забракованными при несоответствии требованиям НД по:
1) внешнему виду,
3) подлинности и количественному содержанию лекарственных веществ,
4) наличию видимых механических включений,
5) недопустимых отклонений от номинального объема раствора,
6) нарушению фиксированности укупорки,
7) нарушению действующих требований к оформлению лекарственных средств, предназначенных к отпуску.
Инъекционные растворы должны храниться в соответствии с физико-химическими свойствами лекарственных веществ и установленными приказом МЗ РФ N 214 сроками.
Изготовление стерильных растворов запрещается при отсутсвии данных:
— о химической несовместимости входящих в них лекарственных веществ;
— технологии и режиме стерилизации, а также – отсутствии методик анализа для их полного химического контроля.
3.5. Оформление растворов для инъекций:
этикетка с синей или голубой полосой, надпись «Для инъекций». Указывают N аптеки, фамилию больного, наименование и концентрацию раствора, объем, стерильность «Стерильно», «Приготовлено асептически», N анализа, N рецепта, дату, срок годности, способ применения.
Rp: Sol.Natrii chloridi 0,9%-50ml
D.S. Для в/в инъекций.
К хлориду натрия предъявляется требование апирогенности. Предварительно порошок стерилизуют (прокаливают) в стерильной таре слоем 1-2 см. при 180`С — 2 часа для разрушения пирогенных веществ. Лекарственное средство термостабильное, готовят раствор без стабилизатора.
I.способ — в мерной посуде
ППК: Aquae pro injectionibus q.s.
Natrii chloridi 0,45
Aquae pro injectionibus ad 50ml
 V об.= 50 мл
V об.= 50 мл
( в журнале постадийного контроля )
II.способ — без мерной посуды
C max = N / КУО = 4/0,33 = 12,1%
Дата добавления: 2015-06-12 ; просмотров: 3768 . Нарушение авторских прав
Изготовление инъекционных растворов в аптеке (стр. 2 из 3)
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
Новосибирский государственный
медицинский университет
Кафедра фармацевтической технологии и биотехнологии
Тема: «Изготовление растворов для инъекций и инфузий в аптеках»Новосибирск
2014 г.
I. Введение…………………………………………………………………………2
II. Цели и задачи…………………………………………………………………..3
III. Инъекционные растворы как лекарственная форма………………………..3
IV. Стадии технологического процесса…………………………………………4
1) Подготовительные работы………………………………………………. 5
2) Изготовлениераствора…………………………………………………. 17
3) Фильтрование и фасовка…………………. …………………………….24
4) Стерилизация раствора……………………………………………..…….26
5) Контроль качества готовой продукции………………………….………30
6) Оформление к отпуску………………………………………..………….33
Заключение……………………. ………………………………………………..35
Используемая литература………………………………….……………………36I.Введение
Одной из важнейших дозированных лекарственных форма являются растворы для инъекций — solutiones pro injectionibus.
Раствор для инъекций — жидкая лекарственная форма, полученная путем растворения одного или нескольких лекарственных веществ, предназначенная для инъекционного применения.
Широта применения инъекционных растворов обусловлена сравнительно большей действенностью искоростью наступления эффекта при парентеральном введении лекарственных веществ. Это объясняется тем, что при данном способе введении лекарственные вещества попадают непосредственно во внутренние среды организма, минуя естественные барьеры. Тем самым, во-первых, ускоряется наступление фармакологического эффекта; во-вторых, увеличивается точность дозировки, так как устраняются те естественные потерилекарственного вещества, которые неизбежны при всасывании его слизистой оболочкой системы пищеварения; в-третьих, вещество, реагируя с тканями организма массою всей своей дозой (особенно при внутривенном введении), обусловливает более выраженный эффект, чем при энтеральном пути введения. Еще одним преимуществом этих растворов является то, что инъекции можно делать больному, который не в состоянии принятьлекарственные вещества в силу потери сознания, наличия черепно-лицевого ранения и т.д. Кроме того, ампулированные инъекционные растворы являются формой портативной, удобной для хранения и транспортировки. Все это делает их одной из наиболее приемлемых дозированных лекарственных форм в практике лечебных учреждений самого различного профиля. Массовый выпуск ампул-шприцев еще более расширяет возможности примененияинъекционных растворов в целях неотложной помощи.
Вместе с тем инъекционному способу введения лекарств присущи и недостатки, что должно быть учтено врачами и фармацевтами. Вследствие того, что лекарства вводятся, минуя защитные барьеры организма, возникает опасность его инфицирования, поэтому одним из важнейших требований, предъявляемых к инъекционным лекарствам, является стерильность. Введениенепосредственно в ткань может вызвать изменение осмотического давления, значения рН и другие физиологические нарушения. При этом ощущается резкая боль, жжение, иногда лихорадочные явления. При введении лекарства непосредственно в кровь возникает опасность закупорки мелких кровеносных сосудов твердыми частицами или пузырьками воздуха, размеры которых превышают диаметр сосудов, что является весьмаопасным. В связи с этим к инъекционным лекарствам предъявляются строгие требования, исключающие возможность изменения состава крови и закупорку кровеносных сосудов (эмболии).
II. Цели и задачи курсовой
-Изучить теоретические основы технологии приготовления лекарственных форм для инъекций.
-Познакомиться с последними исследованиями и достижениями в данной области (в.
Чтобы читать весь документ, зарегистрируйся.
Приготовление инъекционных растворов без стабилизаторов
Страницы работы





Фрагмент текста работы
момента изготовления инъекционных растворов прошло 4 часа. Допустил ли студент нарушения технологии инъекционных растворов?
17.Возьми: Раствора натрия бензоата 15% 50 мл
Дай. Обозначь. Для внутривенного вливания по 10 мл.
После изготовления лекарственной формы студент заполнил лицевую сторону паспорта письменного контроля (ППК)
Натрия бензоата 7,5
Воды очищенной 44,5
 Объем 50 мл
Объем 50 мл
Какие ошибки допустил студент?
18. Студент для укупорки инъекционного раствора использовал резиновые пробки, которые простерилизовал в сушильном шкафу при 180°С 60 минут. Оцените действия студента.
19. Возьми: Раствора кальция хлорида 10% 80 мл
Дай. Обозначь. По 10 мл внутривенно.
После изготовления лекарственной формы студент заполнил лицевую сторону ППК
Кальция хлорида 8,0
Воды для инъекций
 Объем 80 мл
Объем 80 мл
Правильно ли студент заполнил ППК?
20. Студент ввиду отсутствия хлорида натрия в асептическом блоке воспользовался находящимся в ассистентской комнате. Правильно ли он поступил?
21.Возьми: Раствора анальгина 25% 50мл
Дай. Обозначь. По 1 мл внутримышечно 3 раза в день.
Студент при изготовлении раствора анальгина в подставку поместил 12,5 г анальгина, добавил 30 мл воды очищенной, после чего профильтровал в склянку для отпуска, укупорил под «обкатку» металлическим колпачком. Простерилизовал при 120° С 8 минут и оформил к отпуску этикетками. Дайте оценку действиям студента.
22.Студент приготовил 300 мл инъекционного раствора в асептических условиях и простерилизовал его при 120°С 8 минут, проверил качество. Какие ошибки допустил студент?
23. Возьми: Раствора натрия хлорида изотонического 100 мл
Студент в асептической комнате в стерильную мерную колбу вместимостью 100 мл поместил 0,9 г натрия хлорида, довел водой для инъекций до метки. Полученный раствор профильтровал через один слой марли в склянку для отпуска. Простерилизовал при 100°С 30 минут. Оформил к отпуску. Правильно ли приготовлена лекарственная форма.
24.При изготовлении 250 мл инъекционного раствора студент растворил прописанные ингредиенты в воде очищенной и процедил через бумажный фильтр в склянку для отпуска, проверил качество. Оформил соответствующими этикетками. Оцените действия студента.
Задание 3 Опишите по форме рецепты.
Образец оформления рецепта.
1. Возьми: Раствора анальгина 25% 30 мл
Дай. Обозначь. По 1 мл внутримышечно 3 раза в день.
1.1. Rp.: Solutionis Analgini 25% 30 ml
Da. Signa. По 1 мл внутримышечно 3 раза вдень.
1.2. Свойства ингредиентов.
Analginum – белый или белый с едава заметным желтоватым оттенком крупноигольчатый кристаллический порошок, легко растворим в воде (ГФ Х, ст. 57)
1.3. Ингредиенты совместимы.
1.4. Характеристика лекарственной формы.
Жидкая лекарственная форма для инъекционного применения, представляющая собой истинный раствор, в состав которого входит вещество списка Б.
1.5. Проверка доз вещества списка А и Б и норм одноразового отпуска.
Высшие дозы анальгина для внутримышечного введения по ГФ Х.
В 1 мл 25% раствора анальгина содержится 0,25
разовая доза 0,25
Суточная доза 0,25´3=0,75
Дозы не завышены. Рецепт выписан правильно, оформлен штампом и печатью ЛПУ «Для рецептов».
1.6. Паспорт письменного контроля
Оборотная сторона
Воды для инъекций
30 — (7,5´0,68)=24,9 мл
0,68 – коэффициент увеличения объема анальгина
1.7. Технология лекарственной формы с теоретическим обоснованием.
В рецепте прописан раствор вещества, хорошо растворимого в воде, для перентерального применения. Раствор готовят весо-объемным способом в асептических условиях (приказ МЗ РФ № 309 от 21.10.97) для обеспечения минимального загрязнения раствора микроорганизмами.
Создание асептических условий достигается приготовлением инъекционных лекарств из стерильных медикаментов, в стерильной посуде и в специально оборудованном помещении. Однако асептика не может гарантировать полную стерильность растворов, поэтому они в дальнейшем подвергаются стерилизации.
При расчете количества воды для инъекций необходимо учитывать, что концентрация анальгина превышает 3% и согласно приказа МЗ РФ № 308 от 21.10.97 необходимо учитывать коэффициент увеличения объема.
В асептическом блоке в стерильной подставке в 34,65 мл свежеперегнанной воды для инъекций растворяют 7,5 г анальгина (сорта х.ч.). Приготовленный раствор фильтруют через двойной стерильный беззольный
ТЕМА: ИЗГОТОВЛЕНИЕ ИНЪЕКЦИОННЫХ РАСТВОРОВ БЕЗ СТАБИЛИЗАТОРОВ
1. Значимость изучаемой темы.
Инъекционный способ введения лекарств получил в настоящее время широкое применение, поскольку этот способ введения обеспечивает быстрое действие лекарства, которое минует при этом разрушающее действие желудочно-кишечного тракта и печени. Введением лекарства непосредственно в кровяное русло или ткани объясняются требования, предъявляемые к лекарственным формам для инъекций: стерильность, стабильность, отсутствие механических включений, апирогенность, а к отдельным инъекционным растворам – изотоничность. Выполнение требований, предъявляемых к инъекционным растворам, предусматривает их обязательное изготовление в асептических условиях. Соблюдение условий асептики, умение проводить стерилизацию приготовленных лекарственных форм, имеет большое значение для практической деятельности провизора-технолога. Знание и навыки практической работы, приобретенные при изготовлении жидких лекарственных форм могут быть использованы при приготовлении лекарственных форм данного раздела.
Уметь готовить инъекционные растворы без стабилизаторов и оценивать их качество.
2.1. Целевые задачи:
ü требования, предъявляемые к инъекционным лекарственным формам и способы их обеспечения;
ü требования нормативных документов по приготовлению, оценке качества, хранению и оформлению к отпуску инъекционных растворов из аптек;
ü способы стерилизации, устройство и правила эксплуатации автоклава.
ü рассчитывать количества лекарственных веществ и воды для инъекций;
ü проводить при необходимости расчет изотонических концентраций;
ü зная свойства входящих в пропись ингредиентов выбирать и обосновывать оптимальную технологию инъекционных растворов;
ü проводить основные технологические операции: отвешивание, отмеривание, растворение, фильтрацию, стерилизацию;
ü оценивать качество инъекционных растворов;
ü оформлять лекарственную форму к отпуску.
3. Вопросы, отражающие содержание занятия
1. Характеристика инъекционных растворов и требования, предъявляемые к ним.
2. Вода для инъекций, требования, предъявляемые к ней, способы получения, условия и сроки хранения. Аппаратура, используемая для получения воды для инъекций.
3. Асептика, асептические условия приготовления лекарственных форм, устройство асептического блока.
4. Технологическая схема изготовления инъекционных растворов.
5. Способы стерилизации, используемая аппаратура.
6. Оценка качества инъекционных растворов.
7. Упаковка, оформление к отпуску и хранение инъекционных растворов.
4. Самостоятельная внеаудиторная работа студента по подготовке к занятию
4.1. Задания для подготовки к занятию
Задание №1. Изучить учебный материал по теме занятия, приведенный в данных методических указаниях и в рекомендуемой литературе.
Удельный вес инъекционных растворов в аптеках лечебно-профилактических учреждений достигает 50%, несколько ниже в хозрасчетных аптеках. Это объясняется преимуществами инъекционного способа введения. Одним из важных условий приготовления инъекционных растворов является соблюдение условий асептики: изготовление лекарственных форм в асептическом блоке аптеки, использование стерильных растворителей, лекарственных препаратов сорта ч.д.а. или «для инъекций», стерильных вспомогательных материалов, посуды, укупорочных средств. Условия асептики приобретают особо важное значение при изготовлении инъекционных растворов термолабильных веществ, которые не выдерживают термической стерилизации.
Стерильность инъекционных растворов достигается различными способами стерилизации. ГФ рекомендует следующие методы: термические (паровой и воздушный); химические (газовый и стерилизацию растворами), стерилизацию фильтрованием, радиационную стерилизацию.
В качестве растворителя для приготовления инъекционных растворов используют свежеперегнанную воду для инъекций, которую хранят не более 24 часов в асептических условиях. Бактериологический контроль и испытание на пирогенность воды для инъекций проводят в соответствии с требованиями ГФ не реже 2 раз в квартал.
Лекарственные вещества, используемые для изготовления инъекционных лекарственных форм должны отвечать требованиям ГФ, ФС, ВФС, ГОСТ, квалификации х. ч. (химически чистый), ч. д. а. (чистый для анализа). Некоторые вещества подвергают дополнительной очистке и выпускают повышенной чистоты, квалификации «годен для инъекций». Примеси, в последних, могут оказывать токсическое воздействие на организм больного или снижать стабильность инъекционных растворов.
Пригодность некоторых лекарственных веществ для инъекционных растворов определяют на основании дополнительных исследований на чистоту. Кальция хлорид проверяют на растворимость в этаноле (органические примеси и содержание железа); гексаметилентетрамин – на отсутствие аминов, солей аммония и хлороформа; кофеин-бензоат натрия – на отсутствие органических примесей; магния сульфат для инъекций не должен содержать марганца.
Лекарственные вещества не должны содержать примеси, влияющие на их стабильность.
Лекарственные вещества, используемые для приготовления инъекционных растворов, не должны содержать токсичные примеси. Глюкоза и желатин могут содержать пирогенные вещества, поэтому в них определяют тест – дозу на пирогенность в соответствии со статьей ГФ «Поверка на пирогенность». Глюкоза не должна давать пирогенный эффект при внутивенном введении 5% раствора из расчета 10 мг/кг массы кролика.
Стабильность или неизменность состава инъекционных растворов достигается строгим соблюдением условий асептики, подбором оптимальной температуры и времени стерилизации, применением консервантов, позволяющих достигать необходимого эффекта стерилизации при более низких температурах, а также использованием стабилизаторов.
Инъекционные растворы не должны содержать каких-либо механических примесей и быть совершенно прозрачными. Наличие в инъекционном растворе твердых частиц может привести к закупорке сосудов и летальному исходу.
Для освобождения инъекционных растворов от механических примесей их подвергают фильтрованию. С этой целью используют двойные складчатые фильтры из беззольной мелкопористой фильтровальной бумаги с комочком длинноволокнистой ваты. В последнее время широко используются стеклянные фильтры с пористым дном, в этом случае фильтрация проводится под вакуумом.
Приготовление инъекционных растворов без стабилизаторов складывается из следующих последовательных операций:
ü расчет количества воды и сухих лекарственных веществ;
ü отмеривание необходимого количества воды для инъекций и отвешивание лекарственных веществ;
ü подготовка флакона и укупорочных средств;
ü оценка качества инъекционного раствора;
ü оформление к отпуску,
ü оценка качества.
Инъекционные растворы готовят массо-объемным способом (т. к шприцы градуированы по объему) в соответствии с требованием приказа МЗ РФ. При отсутствии мерных сосудов количество растворителя определяют расчетным путем, пользуясь величиной плотности раствора данной концентрации или коэффициентом увеличения объема.
Растворы для инъекций отпускают в стерильных флаконах из нейтрального стекла марки НС-2, НС-1. Для укупорки флаконов используют стерильные резиновые пробки из силиконовой резины, натурального каучука, бутилового каучука. Разрешается использовать стеклянные пробки со шлифом. Флаконы, укупоренные резиновыми пробками, обкатывают металлическими колпачками, флаконы, укупоренные стеклянными пробками, обвязывают пергаментной бумагой. Перед стерилизацией все флаконы маркируют.
Оформление к отпуску растворов для инъекций для амбулаторных больных осуществляется согласно требованиям НД, этикетками синего цвета с указанием состава лекарства, способа применения, даты и условий хранения «Хранить в прохладном, защищенном от света месте», «Беречь от детей».
Хранение инъекционных растворов осуществляют в условиях, исключающих возможность их загрязнения. Срок годности стерильных растворов во флаконах, герметично укупоренных резиновыми пробками «под обкатку», составляет от 7 до 30 суток, а флаконов, укупоренных «под обвязку», не более 2 суток.
Оценку качества растворов для инъекций осуществляют до и после стерилизации. До стерилизации растворы подвергают полному химическому контролю, включая определение рН, изотонирующих и стабилизирующих веществ, контролю на отсутствие механических включений. После стерилизации определяют величину рН, проводят качественный и количественный анализ лекарственных веществ, контролируют отсутствие механических включений качество укупорки. Для контроля отбирается один флакон раствора в каждой серии.
Контроль растворов для инъекций на стерильность и наличие пирогенных веществ осуществляется не реже 2 раз в квартал согласно требованиям ГФ.
Органолептический, опросный, письменный виды контроля, оформление к отпуску готовой лекарственной формы осуществляют согласно требований приказов МЗ и другой НД.
Задание №2. В дневнике описать по форме рецепты, заданные преподавателем. Правильность выполнения задания 2 сравнить с эталоном ответа к рецептурной прописи №1.
1. Возьми: Раствора анальгина 25% 30 мл
Обозначь: По 1 мл внутримышечно 3 раза в день.
1.1. Rp.: Solutionis Analgini 25% 30 ml.
Signa: По 1 мл внутримышечно 3 раза в день.
1.2. Свойства ингредиентов
Analginum – белый или белый с едва заметным желтоватым оттенком крупноигольчатый кристаллический порошок, легко растворим в воде. (ГФ X, ст. 57).
1.3. Ингредиенты совместимы.
1.4. Характеристика лекарственной формы.
Жидкая лекарственная форма для инъекционного применения, представляющая собой истинный раствор.
1.5. Проверка доз и норм одноразового отпуска
Согласно ГФ Х высшие дозы анальгина для внутримышечного введения:
В 1 мл 25% раствора анальгина содержится 0,25
Разовая доза 0,25;
Суточная доза (0,25×3) 0,75
Дозы не завышены. Рецепт выписан правильно, оформлен штампом и печатью лечебно-профилактического учреждения «Для рецептов».
1.6. Паспорт письменного контроля
Дата добавления: 2018-06-01 ; просмотров: 3372 ;
Стадии технологического процесса производства инъекционных растворов, их характеристика
РАСТВОРЫ ДЛЯ ИНЪЕКЦИЙ. ФИЗИОЛОГИЧЕСКИЕ РАСТВОРЫ.
План лекции
Основы латинского языка с медицинской терминологией
Правила выписывания рецептурных прописей
Организация деятельности аптеки и ее структурных подразделений
Приказы регламентирующие правила работы фармацевта по приёму рецептов, изготовлению и хранению лекарственных препаратов
Этапы лекционного занятия
1. Организационный момент
Преподаватель входит в аудиторию, приветствует присутствующих, проверяет отсутствующих. Проверяет готовность аудитории к проведению занятия.
2. Сообщение темы, начальная мотивация, постановка целей и плана лекции.
Преподаватель сообщает название темы: «Растворы для инъекций. Физиологические растворы»
1. Стадии технологического процесса производства инъекционных растворов, их характеристика;
2. Частная технология инъекционных растворов
2.1. Расчет изотонических концентраций растворов с использованием изотонических эквивалентов по натрия хлориду
2.2. Изготовление инъекционных растворов не выдерживающих стерилизацию
2.3. Изготовление инъекционных растворов требующих добавления стабилизатора
2.3.1. Стабилизация растворов лекарственных веществ, подвергающихся гидролизу
2.3.2. Стабилизация растворов легкоокисляющихся веществ
3. Оформление растворов для инъекций.
4. Физиологические растворы
3. Организация и управление учебно-познавательной деятельностью
Преподаватель знакомит студентов с основными вопросами темы
4. Обобщение изложенного материала
В конце занятия подводится итог, что нового узнали студенты, и что было для них повторением
5. Подведение итогов, задание на дом
После прочтения лекции студентам сообщается, что следующая тема будет называться «Глазные лекарственные формы»
Литература: Учебник фарм. технологии И.И. Краснюк, 2004, с.187-225
План лекции:
1. Стадии технологического процесса производства инъекционных растворов, их характеристика;
2. Частная технология инъекционных растворов
2.1. Расчет изотонических концентраций растворов с использованием изотонических эквивалентов по натрия хлориду
2.2. Изготовление инъекционных растворов не выдерживающих стерилизацию
2.3. Изготовление инъекционных растворов требующих добавления стабилизатора
2.3.3. Стабилизация растворов лекарственных веществ, подвергающихся гидролизу
2.3.4. Стабилизация растворов легкоокисляющихся веществ
3. Оформление растворов для инъекций.
4. Физиологические растворы
Технологический процесс производства инъекционных растворов в условиях аптеки складывается из следующих стадий:
1) Подготовительные работы.
2) Изготовление раствора.
3) Фильтрование и фасовка.
1. На подготовительной стадии, проводятся работы по созданию условий асептики, которые включают подготовку помещения, персонала, вспомогательных материалов, оборудования, тароупаковочных средств в соответствии с требованиями действующей НД, подготовка лекарственных веществ, растворителей, приготовление стабилизаторов.
Для получения апирогенной воды могут использоваться аквадистилляторы различной конструкции, например, АА-1, АА-10, АЭВС-4, АЭВС-25, АЭВС-60.
На подготовительной стадии проводятся также расчеты. В отличие от других лекарственных форм практически для всех инъекционных растворов регламентированы составы, а также способы обеспечения их стерильности и стабильности (Приказ МЗ РФ № 214 от 16.07.97, Методические указания по изготовлению стерильных растворов в аптеке, утвержденных МЗ МП РФ 24.08.94).
2. На стадии изготовления раствора проводят отвешивание, отмеривание, а также осуществляют химический контроль раствора. Инъекционные растворы готовят массо-объемным способом (Приказ МЗ РФ № 308 от 21.10.97) в мерной посуде или объем растворителя определяют расчетным путем. Если необходимо, то добавляют стабилизатор, до растворения лекарственного вещества. Затем проводится полный химический контроль
3. Фильтрование и розлив.
После фасовки проводится первичный контроль растворов на отсутствие механических включений, визуально. Контролю подвергается каждый флакон. При обнаружении механических включений раствор перефильтровывают. После проверки на чистоту флаконы, укупоренные резиновыми пробками, обкатывают металлическими колпачками с помощью специальных устройств (например, полуавтомата ЗП-1) и маркируют. Маркировка осуществляется с помощью жетонов, либо название раствора и его концентрация отштамповываются на металлическом колпачке или наносятся несмывающейся краской. Укупорка «под обвязку» допускается в крайнем случае.
4. Стерилизация. Для стерилизации водных растворов лекарственных веществ и воды в аптечных условиях наиболее часто используют один из термических методов — стерилизацию насыщенным паром при 120 0 С и давлении 0,11 МПа с использованием паровых стерилизаторов: вертикальных (ВК-15, ВК-30) и горизонтальных (ГК-100, ГП-280, ГП-400, ГПД-280 и др.) Время стерилизации в зависимости от объема раствора составляет 8-15 мин. Стерилизация растворов более 1 л запрещается. Стерилизация текучим паром при температуре 100 0 С допускается лишь в тех случаях, когда этот метод является единственно возможным для данного раствора.
Растворы термолабильных веществ, не выдерживающих тепловую стерилизацию, изготовляют асептически на стерильной воде для инъекций. Целесообразно с целью стерилизации таких растворов использовать стерильную фильтрацию.
После стерилизации проводят вторичный контроль на отсутствие механических включений, качество укупорки флаконов, физико-химический и полный химический контроль.
Повторная стерилизация растворов для инъекций не допускается.
Выборочно инъекционные лекарственные формы и вода для инъекций проверяются на стерильность и на апирогенность.
5. Стандартизация. После стерилизации проводится повторный контроль на отсутствие видимых механических включений, прозрачность, цветность, а также полный химический анализ (Приказ МЗ РФ № 214 от 16.07.97, ГФ Х1, Т.2.- С.140-143).
Дата добавления: 2014-01-07 ; Просмотров: 3972 ; Нарушение авторских прав?
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Курсовая работа на тему: «Растворы для инъекций, приготовленные в условиях аптеки» 76448
Представленная работа ранее уже была оценена преподавателем нашего клиента на «отлично». Использование данного материала в качестве основы ускорит процесс подготовки Вашего собственного проекта. Можете быть уверены, что работа уникальна, предлагаем ее только мы, и в открытом доступе в интернете она не находится! Еще один плюс: готовая работа в несколько раз дешевле, чем новая.
Содержание
Введение. Растворы для инъекций – практическое значение
- Растворители для приготовления растворов для инъекций
1.1. .Вода для инъекционных растворов
1.2.Другие растворители для инъекционных растворов
2.Изготовление растворов для инъекций в условиях аптеки
2.1.Основные качества инъекционных растворов, изготовляемых
в условиях аптеки
2.2. Специальные требования к инъекционным растворам,
изготовляемым в условиях аптеки
Введение
Актуальность данной темы заключается в том, что инъекционные растворы, являясь традиционными лекарственными формами, не имеют более эффективных аналогов и представляют перспективное направление.
Целью работы является установить особенности инъекционных растворов, особенностей их приготовления в условиях аптеки.
Задачами работы является выяснить особенности приготовления инъекционных растворов.
ГФ XIII издания дает такое определение лекарственной формы Растворы для инъекций в соответствии с ОФС «Лекарственная форма для парентерального применения»:
«Лекарственные формы для инъекций – стерильные лекарственные формы для парентерального применения в виде растворов, суспензий, эмульсий, а также твердых лекарственных веществ (порошки, таблетки, пористые массы), которые растворяют в стерильном растворителе непосредственно перед введением».
Санитарные требования при приготовлении лекарств в асептических условиях регламентируются приказом МЗ РФ № 309 от 21.10.1997г. «Об утверждении инструкции по санитарному режиму аптечных организаций (аптек)».
Различают инъекции малого объема (до 100 мл) и большого объема (100 мл и более – инфузии). Порошки для инъекций – стерильные твердые лекарственные средства, применяемые для приготовления растворов или суспензий для инъекций. Растворы для инъекций – стерильные водные или неводные растворы лекарственных веществ в соответствующем растворителе. Суспензии для инъекций – стерильные высокодисперсные суспензии. Эмульсии для инъекций – стерильные высокодисперсные эмульсии.
Раствор для инъекций (Solutiones pro injectionibus) – это жидкая лекарственная форма для парентерального введения (минуя желудочно-кишечный тракт). Растворы для инъекций вводят подкожно (п/к), внутримышечно (в/м), внутривенно (в/в). Лекарственные формы для инъекций – промышленного производства: ампулы, флаконы, шприц-тюбики. Лекарственные формы для инъекций должны быть стерильными, стойкими, апирогенными, свободными от механических примесей.
При выписывании сокращенной рецептурной прописи на раствор или суспензию в ампулах сначала указывают лекарственную форму и название лекарственного вещества в родительном падеже единственного числа, характер раствора (если он масляный), концентрацию в процентах и количество миллилитров в одной ампуле. После этого указывают количество ампул.
Инъекционные растворы относятся к лекарственным средствам, предназначенным для парентерального применения, поэтому это – это стерильные препараты, которые предназначаются для введения их путем инъекций, инфузий или имплантаций в организм человека. Сюда относят растворы, эмульсии, суспензии, порошки, а также таблетки для изготовления растворов и имплантаций, лиофилизированных препараты, которые вводятся парентерально:
- Подкожно;
- Внутримышечно;
- Внутривенно;
- Внутриартериально — в различные полости.
На настоящем этапе среди всех готовых лекарственных средств, которые выпускаются отечественной фармацевтической промышленностью, доля парентеральных препаратов приходится около 30%. На инъекционные препараты в различных фармакопеях мира приходится от 10% до 15% статей.
В соответствии с ГФ, лекарственными формами для инъекций относятся:
- водные и масляные растворы;
- суспензии и эмульсии;
- стерильные порошки;
- пористые массы и таблетки, которые растворяют в стерильном растворителе непосредственно перед введением.
Водные инъекционные растворы объемом 100 мл и более называют инфузионными.
Если данный вариант Вам не подходит, мы поможем Вам в написании новой работы. Вы можете обратиться к нам с любыми проблемами в учебе! Кроме того, если Вам интересно разобраться в предмете, мы научим Вас самостоятельно решать задачи, подготавливать рефераты, курсовые, дипломы и т.д.



